W wyniku rozwoju cywilizacji technicznej na Ziemi nastąpiło wiele skażeń chemicznych, których obecnie nie można szybko wyeliminować za pomocą filtracji, bądź innych technik chemicznych. Atmosfera planety na terenach miejskich zanieczyszczona jest bardziej niż terenie otwartym. Obieg CO2 w przyrodzie został zakłócony przez wzmagającą się produkcję tej substancji z elektrowni opalanych węglem i węglowodorami. Ma to bezpośredni wpływ na jakość życia ludzi i prowadzi do między innymi chorób nowotworowych. Inne technologie nie oparte na spalaniu węglopochodnych paliw są w mniejszości w porównaniu z globalną produkcją energii. Cykle przyrodnicze typu cyklu z udziałem światła, czyli fotosyntezy będące w równowadze z produkowanym na różne sposoby dwutlenkiem węgla w przeszłości spowodowały wydzielenie go z atmosfery i obecnie w postaci węgla kamiennego i brunatnego zalega on pod Ziemią.Poprzez wydobycie go w procesie prac górniczych i spalanie dochodzi do powrotu tego gazu do atmosfery, co może być w dłuższej perspektywie czasowej przyczyną tego, że następne pokolenia będą zmuszone do wypracowania innych technik pozyskania energii, jeżeli będą chciały przetrwać. Skażenie wód powierzchniowych jest także znaczne, szczególnie śródlądowych. Woda morska jest zanieczyszczona przy wybrzeżach, gdzie ujście mają delty rzek. Tlenki siarki (SO2, SO3) oraz azotu (NO2) zakwaszają hydrosferę. Są miejsca na planecie gdzie zatrucie środowiska przekracza wszelkie normy, pomimo tego żyją tam ludzie, gdyż organizm ludzki może przystosować się jeżeli będzie przyzwyczajany do trujących substancji stopniowo. W atmosferze jest coraz więcej wilgoci i oparów. Na moim osiedlu jesienią i w zimie praktycznie nie można otworzyć okna, zwłaszcza przy bezwietrznej pogodzie, bo powietrze jest tak zanieczyszczone z palenisk opalanych węglem i innymi substancjami, że trudno oddychać. Sytuacja mogłaby ulec zmianie, gdyby można było domknąć cykl produkcji spalin poprzez nie magazynowanie ich pod ziemią, a poprzez przerobienie ich za pomocą sztucznej fotosyntezy z powrotem na tlen i węgiel albo metan, które mogły by po raz kolejny być spalone i cykl by się domknął.
Do tego celu można by również zastosować np. reakcję Sabatiera katalizowaną przez ruten lub reakcje typu Fischera-Tropscha w celu otrzymania węglowodorów z CO i H2. Inne metody to kolejne technologie określane jako tkz. "Green chemistry" polegającą na bezodpadowych reakcjach chemicznych, w procesie których nie powstają produkty uboczne. Większość procesów chemicznych zachodzących w przyrodzie może być wzorcem dla wielu rozwiązań technologicznych w chemii przemysłowej. Adaptacja niektórych z nich to poważne wyzwanie dla nauki. Obieg podstawowych elementów w przyrodzie napędza energia słoneczna. Energia słoneczna, której faktycznie jeżeli brać pod uwagę całkowitą jej wartość produkowaną przez Słońce, a która dociera do Ziemi, jest znikomo mała, reszta marnuje się i jest rozpraszana w bezkresie przestrzeni Układu Słonecznego. Są to wartości energii, którą gdyby udało się jakoś wykorzystać np. magazynując ją w jakichś kryształach, mogła by umożliwić napędy typu WARP i inne obecnie nie stosowane idee z uwagi na ich wymogi technologiczne. Energia produkowana przez elektrownie na świecie, jest wytwarzana z małą sprawnością, na każdym elemencie typu turbiny, prądnicy, generatora pary, następują opory bezwładnościowe i dynamiczne powodujące duże straty energii. .
W przyrodzie fotosynteza zachodzi z udziałem cząsteczki chlorofilu z centralnie położonym atomem magnezu z udziałem światła widzialnego, przy niskich energiach aktywacji progu energetycznego reakcji. Sztuczna fotosynteza w postaci, którą postuluje się obecnie jest procesem o wiele bardziej wymagającym energetycznie, podczas gdy reakcja w przyrodzie zachodzi łatwo, tutaj musimy dostarczyć energii ultrafioletu, czyli energii fali wyższej niż światło widzialne. Skutecznego katalitycznego użycia innych niż chlorofil substancji jak rodopsyna jest wiele i chemia jest bogata w ciekawe rozwiązania zastępcze fotosyntezy, jednak nie widać na razie praktycznego użycia tych technologii na skalę przemysłową, ze szczególnym naciskiem w kierunku "odtrucia" atmosfery z nadmiaru CO2. Innym ciekawym zastosowaniem m.in. biotechnologii, byłoby zastosowanie procesów przyrodniczych do napędu pojazdów w cyklu zamkniętym, z udziałem odpowiednich reakcji chemicznych, które zapewniałyby odzysk spalonego paliwa ze spalin, czyli w tym rozwiązaniu zero emisyjnym, zakładając 100 % sprawności reakcji, byłoby to rozwiązanie typu "free energy". Jednak gdyby rozważać tego typu rozwiązania gdzie tankowanie paliwa, byłoby jednorazową czynnością i później można by jeździć do całkowitego zużycia mechanicznego elementów samochodu, to całość zakrawa już na fantastykę i może być obiektem zainteresowania pisarzy sci-fi. Kiedyś spotkałem się także z opisem urządzeń, które teoretycznie funkcjonują na zasadzie obdzierania z elektronów cząstek powietrza, energia uzyskana tym sposobem miałaby być użyta do zasilania nawet mocno prądożernych urządzeń. Urządzenie tego typu powodowało powstawanie O3 w swoim otoczeniu jako jedyny skutek uboczny jego pracy. Jeżeli chodzi jednak o CO2 to najwięcej zanieczyszczeń emitują koksownie oraz huty - gdzie w procesie przeróbki rudy na stal przy jej redukcji musi utleniany być węgiel, a produktem odpadowym jest dwutlenek węgla. Innymi producentami CO2 są cementownie, bo w procesie uzyskania cementu czy wapna, w produkcji którego powstaje dwutlenek węgla z margla, który składa się w dużej części CaCO3, czyli węglanu wapnia, nie można wyeliminować procesów z produktami końcowymi, z którymi nie wiadomo co zrobić. Innym problemem jest powstawanie dużych ilości popiołów z elektrowni z kotłami węglowymi, ale również na biomasę i spalarni spalających śmieci. .
Wszystkie gazy toksyczne emitowane z palenisk piecowych można rozbić na molekuły podstawowe tj. tlenki azotu, na tlen i azot, przy użyciu katalizatorów, tlenki siarki i węgla po części nie są składnikiem powietrza jak w przypadku tlenków azotu, więc siarka musiałaby być magazynowana i przetwarzana na np. kwas siarkowy (H2SO4) do celów przemysłu chemicznego, węgiel mógłby zostać użyty w celu produkcji tworzyw sztucznych, bądź w celu produkcji benzyny syntetycznej.
Z drugiej strony obecna brudna chemia nie szybko ustąpi miejsca swoim lepszym stronom, bo siłą rzeczy technologia opiera się na węglu i dopóki on będzie - będzie wykorzystywany, gdyż jest on stosunkowo łatwy do pozyskania a to determinuje późniejsze rozwiązania na których stoi obecny przemysł i każdy kto próbuje to zmienić w radykalny sposób eliminując tą sytuację będzie postrzegany jako radykalny głos i nie zostanie udzielony mu poważniejszy udział w sferze decyzyjnej. Za kilkaset, a może nawet już tylko za kilkadziesiąt lat będzie musiał nastąpić nieuchronny odwrót na całej linii frontu z paliw jakie znamy, bo ceny ich na skutek gwałtownego zmniejszania się ich zasobów w niedalekiej przyszłości wzrosną tak, że nikt nie będzie w stanie utrzymać samochodów, które staną się tylko zabawkami dla ekscentrycznych bogaczy, których będzie na nie stać. Nie będzie też miejsca na elektrownie opalane węglem ani innymi paliwami kopalnymi, a prąd będzie wytwarzany ze źródeł, które obecnie tylko dopiero zarysowują się na horyzoncie technologicznym współczesności. Jakie to będą źródła zależne będzie od wielu wydarzeń, które nastąpią, a których nie sposób obecnie przewidzieć.
Inne technologie nie oparte na spalaniu węglopochodnych paliw są w mniejszości w porównaniu z globalną produkcją energii. Cykle przyrodnicze typu cyklu z udziałem światła, czyli fotosyntezy będące w równowadze z produkowanym na różne sposoby dwutlenkiem węgla w przeszłości spowodowały wydzielenie go z atmosfery i obecnie w postaci węgla kamiennego i brunatnego zalega on pod Ziemią.Poprzez wydobycie go w procesie prac górniczych i spalanie dochodzi do powrotu tego gazu do atmosfery, co może być w dłuższej perspektywie czasowej przyczyną tego, że następne pokolenia będą zmuszone do wypracowania innych technik pozyskania energii, jeżeli będą chciały przetrwać. Skażenie wód powierzchniowych jest także znaczne, szczególnie śródlądowych. Woda morska jest zanieczyszczona przy wybrzeżach, gdzie ujście mają delty rzek. Tlenki siarki (SO2, SO3) oraz azotu (NO2) zakwaszają hydrosferę. Są miejsca na planecie gdzie zatrucie środowiska przekracza wszelkie normy, pomimo tego żyją tam ludzie, gdyż organizm ludzki może przystosować się jeżeli będzie przyzwyczajany do trujących substancji stopniowo. W atmosferze jest coraz więcej wilgoci i oparów. Na moim osiedlu jesienią i w zimie praktycznie nie można otworzyć okna, zwłaszcza przy bezwietrznej pogodzie, bo powietrze jest tak zanieczyszczone z palenisk opalanych węglem i innymi substancjami, że trudno oddychać. Sytuacja mogłaby ulec zmianie, gdyby można było domknąć cykl produkcji spalin poprzez nie magazynowanie ich pod ziemią, a poprzez przerobienie ich za pomocą sztucznej fotosyntezy z powrotem na tlen i węgiel albo metan, które mogły by po raz kolejny być spalone i cykl by się domknął.
Do tego celu można by również zastosować np. reakcję Sabatiera katalizowaną przez ruten lub reakcje typu Fischera-Tropscha w celu otrzymania węglowodorów z CO i H2. Inne metody to kolejne technologie określane jako tkz. "Green chemistry" polegającą na bezodpadowych reakcjach chemicznych, w procesie których nie powstają produkty uboczne. Większość procesów chemicznych zachodzących w przyrodzie może być wzorcem dla wielu rozwiązań technologicznych w chemii przemysłowej. Adaptacja niektórych z nich to poważne wyzwanie dla nauki. Obieg podstawowych elementów w przyrodzie napędza energia słoneczna. Energia słoneczna, której faktycznie jeżeli brać pod uwagę całkowitą jej wartość produkowaną przez Słońce, a która dociera do Ziemi, jest znikomo mała, reszta marnuje się i jest rozpraszana w bezkresie przestrzeni Układu Słonecznego. Są to wartości energii, którą gdyby udało się jakoś wykorzystać np. magazynując ją w jakichś kryształach, mogła by umożliwić napędy typu WARP i inne obecnie nie stosowane idee z uwagi na ich wymogi technologiczne. Energia produkowana przez elektrownie na świecie, jest wytwarzana z małą sprawnością, na każdym elemencie typu turbiny, prądnicy, generatora pary, następują opory bezwładnościowe i dynamiczne powodujące duże straty energii. .
W przyrodzie fotosynteza zachodzi z udziałem cząsteczki chlorofilu z centralnie położonym atomem magnezu z udziałem światła widzialnego, przy niskich energiach aktywacji progu energetycznego reakcji. Sztuczna fotosynteza w postaci, którą postuluje się obecnie jest procesem o wiele bardziej wymagającym energetycznie, podczas gdy reakcja w przyrodzie zachodzi łatwo, tutaj musimy dostarczyć energii ultrafioletu, czyli energii fali wyższej niż światło widzialne. Skutecznego katalitycznego użycia innych niż chlorofil substancji jak rodopsyna jest wiele i chemia jest bogata w ciekawe rozwiązania zastępcze fotosyntezy, jednak nie widać na razie praktycznego użycia tych technologii na skalę przemysłową, ze szczególnym naciskiem w kierunku "odtrucia" atmosfery z nadmiaru CO2. Innym ciekawym zastosowaniem m.in. biotechnologii, byłoby zastosowanie procesów przyrodniczych do napędu pojazdów w cyklu zamkniętym, z udziałem odpowiednich reakcji chemicznych, które zapewniałyby odzysk spalonego paliwa ze spalin, czyli w tym rozwiązaniu zero emisyjnym, zakładając 100 % sprawności reakcji, byłoby to rozwiązanie typu "free energy". Jednak gdyby rozważać tego typu rozwiązania gdzie tankowanie paliwa, byłoby jednorazową czynnością i później można by jeździć do całkowitego zużycia mechanicznego elementów samochodu, to całość zakrawa już na fantastykę i może być obiektem zainteresowania pisarzy sci-fi. Kiedyś spotkałem się także z opisem urządzeń, które teoretycznie funkcjonują na zasadzie obdzierania z elektronów cząstek powietrza, energia uzyskana tym sposobem miałaby być użyta do zasilania nawet mocno prądożernych urządzeń. Urządzenie tego typu powodowało powstawanie O3 w swoim otoczeniu jako jedyny skutek uboczny jego pracy. Jeżeli chodzi jednak o CO2 to najwięcej zanieczyszczeń emitują koksownie oraz huty - gdzie w procesie przeróbki rudy na stal przy jej redukcji musi utleniany być węgiel, a produktem odpadowym jest dwutlenek węgla. Innymi producentami CO2 są cementownie, bo w procesie uzyskania cementu czy wapna, w produkcji którego powstaje dwutlenek węgla z margla, który składa się w dużej części CaCO3, czyli węglanu wapnia, nie można wyeliminować procesów z produktami końcowymi, z którymi nie wiadomo co zrobić. Innym problemem jest powstawanie dużych ilości popiołów z elektrowni z kotłami węglowymi, ale również na biomasę i spalarni spalających śmieci. .
Wszystkie gazy toksyczne emitowane z palenisk piecowych można rozbić na molekuły podstawowe tj. tlenki azotu, na tlen i azot, przy użyciu katalizatorów, tlenki siarki i węgla po części nie są składnikiem powietrza jak w przypadku tlenków azotu, więc siarka musiałaby być magazynowana i przetwarzana na np. kwas siarkowy (H2SO4) do celów przemysłu chemicznego, węgiel mógłby zostać użyty w celu produkcji tworzyw sztucznych, bądź w celu produkcji benzyny syntetycznej.
Z drugiej strony obecna brudna chemia nie szybko ustąpi miejsca swoim lepszym stronom, bo siłą rzeczy technologia opiera się na węglu i dopóki on będzie - będzie wykorzystywany, gdyż jest on stosunkowo łatwy do pozyskania a to determinuje późniejsze rozwiązania na których stoi obecny przemysł i każdy kto próbuje to zmienić w radykalny sposób eliminując tą sytuację będzie postrzegany jako radykalny głos i nie zostanie udzielony mu poważniejszy udział w sferze decyzyjnej. Za kilkaset, a może nawet już tylko za kilkadziesiąt lat będzie musiał nastąpić nieuchronny odwrót na całej linii frontu z paliw jakie znamy, bo ceny ich na skutek gwałtownego zmniejszania się ich zasobów w niedalekiej przyszłości wzrosną tak, że nikt nie będzie w stanie utrzymać samochodów, które staną się tylko zabawkami dla ekscentrycznych bogaczy, których będzie na nie stać. Nie będzie też miejsca na elektrownie opalane węglem ani innymi paliwami kopalnymi, a prąd będzie wytwarzany ze źródeł, które obecnie tylko dopiero zarysowują się na horyzoncie technologicznym współczesności. Jakie to będą źródła zależne będzie od wielu wydarzeń, które nastąpią, a których nie sposób obecnie przewidzieć.
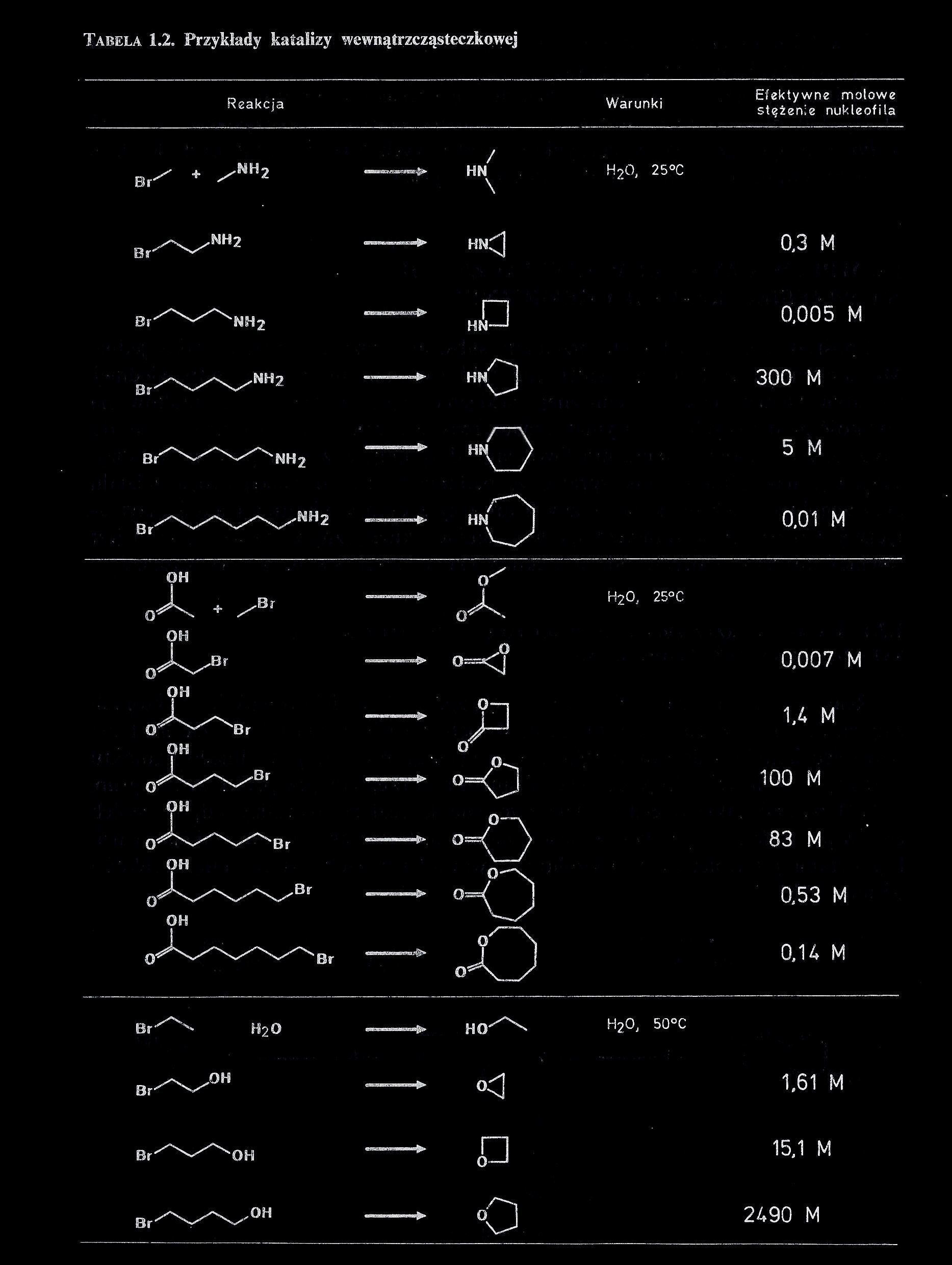
| Kataliza wewnątrzcząsteczkowa |
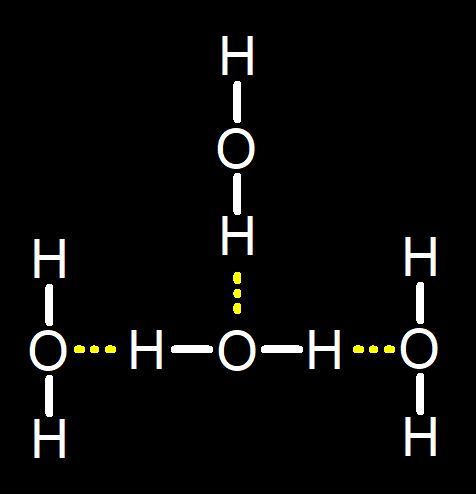
Tlenek wodoru potocznie znany pod nazwą wody, zalega w postaci oceanów na 75 % powierzchni planety Ziemi. Woda zawdzięcza swoje właściwości m.in. mostkom wodorowym. Co to są mostki wodorowe ? Mostki wodorowe to tworzące się w wodzie oddziaływania pomiędzy spolaryzowanymi cząsteczkami tlenku wodoru. Mostki wodorowe maja wpływ na większą spoistość wody, wpływają na końcową temperaturę wrzenia i parowania tej cieczy. Ładunki elektryczne w cząsteczce wody nie są rozłożone równomiernie dlatego właśnie powstają mostki wodorowe i tworzą się one w ten sposób, że spolaryzowane cząsteczki wody starają się przyciągać razem zawsze gdy dochodzi do ich zbliżenia, spolaryzowanymi dodatnie końcami cząsteczki wody i jej ujemnie spolaryzowanymi środkami, gdzie znajduje się atom tlenu, ten efekt sprawia że woda ma jedyne w swoim rodzaju właściwości warunkujące życie zwierząt wodnych i inne zapewniające życie komórek, dla których jest ona medium, w którym dochodzi do sekrecji białek i replikacji kwasu deoksyrybonukleinowego (DNA). Woda stanowi jeden z elementów ekosystemu planety, który ma decydujące znaczenie o jej klimacie, warunkach bytowych dla organizmów żywych i stanowi podstawową substancję, bez której nie mogłoby w ogóle wyewoluować życie, które jest znane obecnie. Woda wchodzi w skład węglowodanów, które tworzą tkankę roślinną, substancji takich jak celuloza, lignina i skrobia.
Karbid, czyli węglik wapnia (wzór sumaryczny CaC2) może być źródłem acetylenu (C2H2) np. w reakcji z wodą:
CaC2+ 2H2O ==> Ca(OH)2 + C2H2. Acetylen stosowany jest do cięcia wysokotemperaturowego różnych metali o wysokich temperaturach topnienia i wraz z tlenem w mieszance można uzyskać temperaturę płomienia nawet 3100 st. C, pozwala to na cięcie metali takich jak stal domieszkowana, nikiel, a nawet chrom i wanad. Acetylen reaguje z wodą bromową i odbarwia ją, na skutek przyłączania się bromu do cząsteczek acetylenu, w procesie tym traci on potrójne wiązanie przechodząc w 1,2-dibromoeten (wiązanie podwójne) i dalej w 1,1,2,2 - tetrabromoetan (całkowicie wysycony).
Dysocjacja elektrolityczna wody, przy której woda rozkłada się na jon wodorotlenkowy i hydroksoniowy.

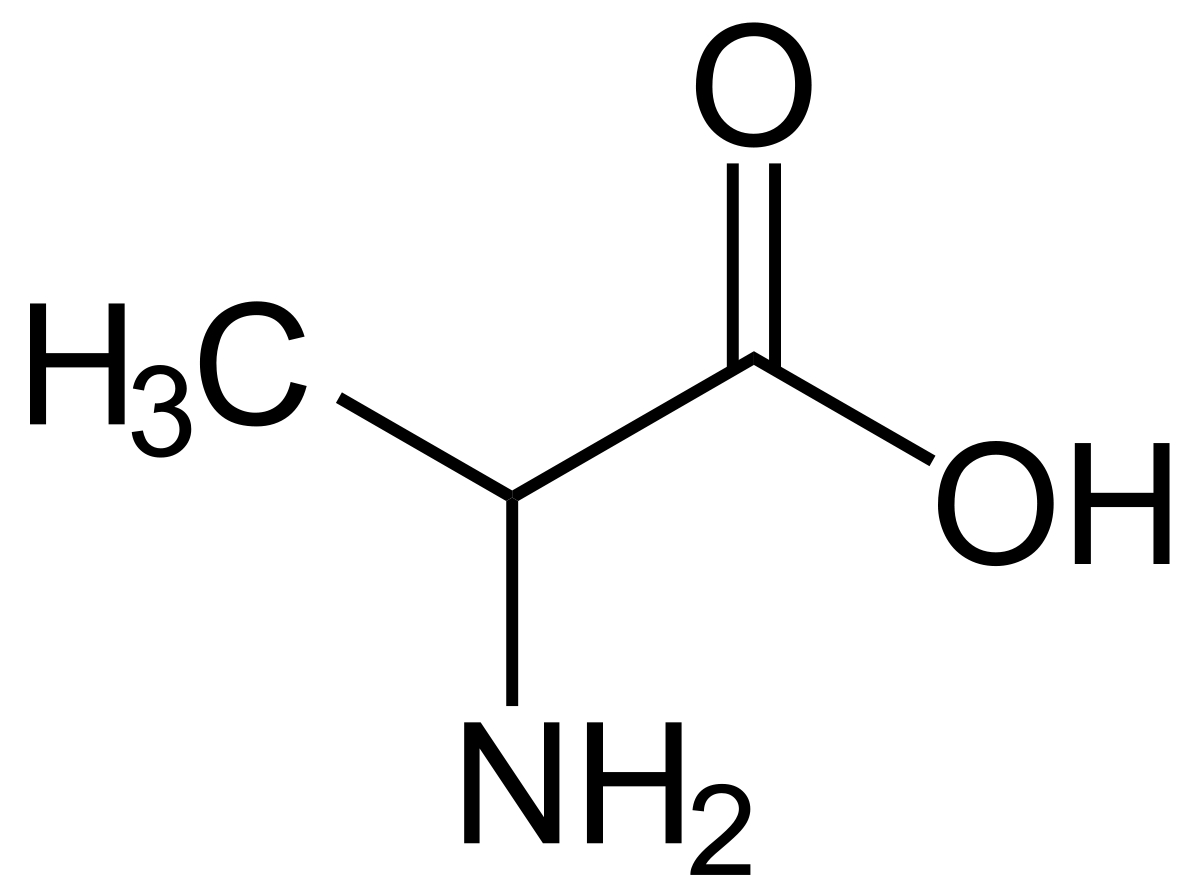
Węgiel jako pierwiastek o liczbie atomowej 12, posiada kilka ważnych izotopów używanych np. w określaniu wieku różnych substancji jak węgiel C 14, który jest izotopem z rozpadem połowicznym o okresie 5730 +/- 40 lat. Węgiel jako pierwiastek powstał tak jak i inne lżejsze pierwiastki w wyniku przemian jądrowych w gwiazdach. We wszechświecie pierwiastek ten jest najprawdopodobniej najbardziej podstawowym i powszechnym budulcem organizmów żywych. Wchodzi on w skład łańcuchów DNA (kwasu deoksyrybonukleinowego), który jest odpowiedzialny za przekazywanie cech genetycznych w organizmach żywych. Wraz z azotem, wodorem, fosforem i tlenem tworzy cegiełki DNA - nukleotydy, które składają się na podstawowy kod życia, adeninę, guaninę, cytozynę i tyminę. Te zaś łączą się między sobą w ściśle określony sposób - adenina tylko z tyminą, cytozyna tylko z guaniną. Mimo że liczba nukleotydów wynosi 4, to zgrupowane trójkami, umożliwiają zapis wszystkich potrzebnych białek, które są podstawowym budulcem w wielu organizmach. Istnieje poza tym duża liczba kombinacji genów nie kodująca żadnego białka. Węgiel uczestniczy i jest jednym z podstawowych składników procesu uzyskania energii w gwiazdach w tkz. cyklu CNO. Ilość kombinacji związków węgla gdy spojrzeć na to z punktu widzenia chemii jego związków, przekracza prawdopodobnie ilość wszystkich innych kombinacji związków chemicznych złożonych z pozostałych pierwiastków w układzie okresowym, gdyż ma on zdolność do łączenia się z czterema przy strukturze tetraedru jak w diamencie, trzema (grafen), struktura plastra miodu, lub dwoma jak w acetylenie, innymi atomami węgla jednocześnie. Węgiel jest pierwiastkiem tworzącym wiele odmian alotropowych typu diamentu, grafenu, fulerenów, czy grafitu. Grafit wykazuje wysoką anizotropię przestrzenną, jest tym twardszy im większy jest kąt jego obróbki. Diament jest najtwardszym minerałem powstałym w warunkach naturalnych w przyrodzie. W przyrodzie w królestwie roślin węgiel wchodzi w skład cząsteczki chlorofilu i wraz z magnezem odpowiedzialny jest za proces fotosyntezy roślin. Tlen to pierwiastek o liczbie atomowej 16, jest na Ziemi produktem ubocznym rozwoju wczesnych organizmów oceanicznych jak również produkowany jest w organellach komórkowych roślin - chloroplastach na masową skalę w roślinach zielonych przy udziale energii słonecznej. Obecnie zawartość tlenu w atmosferze nie przekracza 22 %, jednak dawniej w okresie intensywnego rozwoju roślin - paprotników i skrzypów jego zawartość w atmosferze przekraczała 34 %. Azot w atmosferze pełni rolę niepalnego gazu - nie podtrzymuje on procesu spalania, w odróżnieniu do tlenu, w normalnych warunkach, zapobiega to niekontrolowanemu spalaniu się łatwopalnych substancji w zubożonej w tlen mieszance atmosferycznej. Stanowi on około 78 % atmosfery Ziemskiej. Azot wchodzi w skład białek, enzymów, w zasadzie wszystkich substancji białkowych w organizmach żywych, czyli aminokwasów składających się na polipeptydy, bo jak sama nazwa wskazuje aminokwas jest to połączenie grupy aminowej (NH2) z grupą karboksylową o wzorze sumarycznym(-COOH), jednym z prostszych aminokwasem jest glicyna (NH2CH2COOH) lub alanina (CH3CH(NH2)COOH). Azot jest składnikiem hydrazyny, która stanowi dobre acz szkodliwe dla człowieka paliwo rakietowe do rakiet. Poza tym azot w pewnych związkach stosowany jest do produkcji azotku galu, gdzie w procesie wysokociśnieniowej krystalizacji może dochodzić do krystalizacji tej substancji, która może posłużyć do budowy elektroniki o znacznie polepszonych parametrach. Innym zastosowaniem azotu jest wykorzystanie w przemyśle materiałów wybuchowych. Substancje które zawierają azot to m. in. trotyl, nitrogliceryna, C4, Semtex i wiele innych.
| Alanina wzór sumaryczny: CH3CH(NH2)COOH i półstrukturalny |

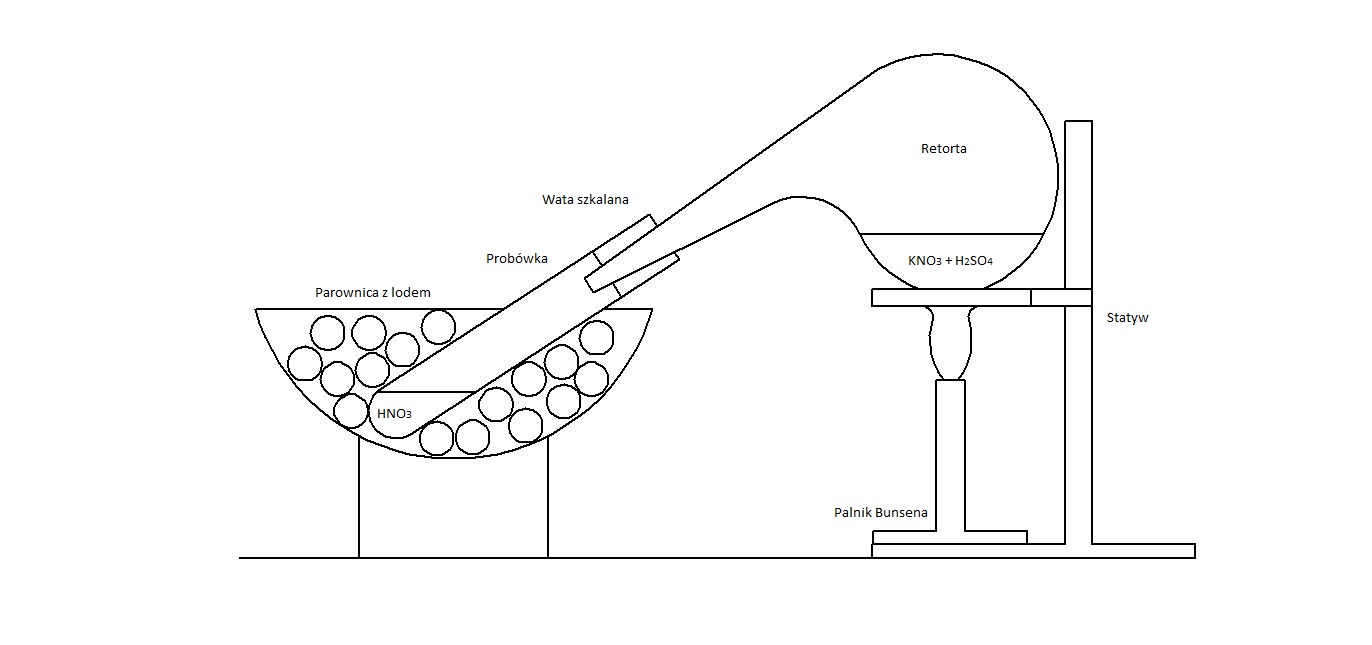
Wytwarzanie kwasu azotowego (HNO3) w warunkach małego laboratorium. Do doświadczenia użyjemy azotanu potasu (KNO3)dostępnego powszechnie w sklepach spożywczych i stosowanego do mięs w kuchni, oraz stężonego kwasu siarkowego (H2SO4). Stężony kwas siarkowy należy zmieszać z azotanem potasu i powstałą mieszankę ogrzewać w retorcie palnikiem Bunsena. Końcówka retorty powinna wchodzić w probówkę, ochładzaną w parownicy z lodem. Wylot probówki dodatkowo zabezpieczamy watą szklaną. Opary wydostające się z retorty skraplają się na zimnych ścianach probówki, jest to stężony kwas azotowy tkz. dymiący kwas azotowy.

 Inne technologie nie oparte na spalaniu węglopochodnych paliw są w mniejszości w porównaniu z globalną produkcją energii. Cykle przyrodnicze typu cyklu z udziałem światła, czyli fotosyntezy będące w równowadze z produkowanym na różne sposoby dwutlenkiem węgla w przeszłości spowodowały wydzielenie go z atmosfery i obecnie w postaci węgla kamiennego i brunatnego zalega on pod Ziemią.Poprzez wydobycie go w procesie prac górniczych i spalanie dochodzi do powrotu tego gazu do atmosfery, co może być w dłuższej perspektywie czasowej przyczyną tego, że następne pokolenia będą zmuszone do wypracowania innych technik pozyskania energii, jeżeli będą chciały przetrwać. Skażenie wód powierzchniowych jest także znaczne, szczególnie śródlądowych. Woda morska jest zanieczyszczona przy wybrzeżach, gdzie ujście mają delty rzek. Tlenki siarki (SO2, SO3) oraz azotu (NO2) zakwaszają hydrosferę. Są miejsca na planecie gdzie zatrucie środowiska przekracza wszelkie normy, pomimo tego żyją tam ludzie, gdyż organizm ludzki może przystosować się jeżeli będzie przyzwyczajany do trujących substancji stopniowo. W atmosferze jest coraz więcej wilgoci i oparów. Na moim osiedlu jesienią i w zimie praktycznie nie można otworzyć okna, zwłaszcza przy bezwietrznej pogodzie, bo powietrze jest tak zanieczyszczone z palenisk opalanych węglem i innymi substancjami, że trudno oddychać. Sytuacja mogłaby ulec zmianie, gdyby można było domknąć cykl produkcji spalin poprzez nie magazynowanie ich pod ziemią, a poprzez przerobienie ich za pomocą sztucznej fotosyntezy z powrotem na tlen i węgiel albo metan, które mogły by po raz kolejny być spalone i cykl by się domknął.
Do tego celu można by również zastosować np. reakcję Sabatiera katalizowaną przez ruten lub reakcje typu Fischera-Tropscha w celu otrzymania węglowodorów z CO i H2. Inne metody to kolejne technologie określane jako tkz. "Green chemistry" polegającą na bezodpadowych reakcjach chemicznych, w procesie których nie powstają produkty uboczne. Większość procesów chemicznych zachodzących w przyrodzie może być wzorcem dla wielu rozwiązań technologicznych w chemii przemysłowej. Adaptacja niektórych z nich to poważne wyzwanie dla nauki. Obieg podstawowych elementów w przyrodzie napędza energia słoneczna. Energia słoneczna, której faktycznie jeżeli brać pod uwagę całkowitą jej wartość produkowaną przez Słońce, a która dociera do Ziemi, jest znikomo mała, reszta marnuje się i jest rozpraszana w bezkresie przestrzeni Układu Słonecznego. Są to wartości energii, którą gdyby udało się jakoś wykorzystać np. magazynując ją w jakichś kryształach, mogła by umożliwić napędy typu WARP i inne obecnie nie stosowane idee z uwagi na ich wymogi technologiczne. Energia produkowana przez elektrownie na świecie, jest wytwarzana z małą sprawnością, na każdym elemencie typu turbiny, prądnicy, generatora pary, następują opory bezwładnościowe i dynamiczne powodujące duże straty energii. .
W przyrodzie fotosynteza zachodzi z udziałem cząsteczki chlorofilu z centralnie położonym atomem magnezu z udziałem światła widzialnego, przy niskich energiach aktywacji progu energetycznego reakcji. Sztuczna fotosynteza w postaci, którą postuluje się obecnie jest procesem o wiele bardziej wymagającym energetycznie, podczas gdy reakcja w przyrodzie zachodzi łatwo, tutaj musimy dostarczyć energii ultrafioletu, czyli energii fali wyższej niż światło widzialne. Skutecznego katalitycznego użycia innych niż chlorofil substancji jak rodopsyna jest wiele i chemia jest bogata w ciekawe rozwiązania zastępcze fotosyntezy, jednak nie widać na razie praktycznego użycia tych technologii na skalę przemysłową, ze szczególnym naciskiem w kierunku "odtrucia" atmosfery z nadmiaru CO2. Innym ciekawym zastosowaniem m.in. biotechnologii, byłoby zastosowanie procesów przyrodniczych do napędu pojazdów w cyklu zamkniętym, z udziałem odpowiednich reakcji chemicznych, które zapewniałyby odzysk spalonego paliwa ze spalin, czyli w tym rozwiązaniu zero emisyjnym, zakładając 100 % sprawności reakcji, byłoby to rozwiązanie typu "free energy". Jednak gdyby rozważać tego typu rozwiązania gdzie tankowanie paliwa, byłoby jednorazową czynnością i później można by jeździć do całkowitego zużycia mechanicznego elementów samochodu, to całość zakrawa już na fantastykę i może być obiektem zainteresowania pisarzy sci-fi. Kiedyś spotkałem się także z opisem urządzeń, które teoretycznie funkcjonują na zasadzie obdzierania z elektronów cząstek powietrza, energia uzyskana tym sposobem miałaby być użyta do zasilania nawet mocno prądożernych urządzeń. Urządzenie tego typu powodowało powstawanie O3 w swoim otoczeniu jako jedyny skutek uboczny jego pracy. Jeżeli chodzi jednak o CO2 to najwięcej zanieczyszczeń emitują koksownie oraz huty - gdzie w procesie przeróbki rudy na stal przy jej redukcji musi utleniany być węgiel, a produktem odpadowym jest dwutlenek węgla. Innymi producentami CO2 są cementownie, bo w procesie uzyskania cementu czy wapna, w produkcji którego powstaje dwutlenek węgla z margla, który składa się w dużej części CaCO3, czyli węglanu wapnia, nie można wyeliminować procesów z produktami końcowymi, z którymi nie wiadomo co zrobić. Innym problemem jest powstawanie dużych ilości popiołów z elektrowni z kotłami węglowymi, ale również na biomasę i spalarni spalających śmieci. .
Wszystkie gazy toksyczne emitowane z palenisk piecowych można rozbić na molekuły podstawowe tj. tlenki azotu, na tlen i azot, przy użyciu katalizatorów, tlenki siarki i węgla po części nie są składnikiem powietrza jak w przypadku tlenków azotu, więc siarka musiałaby być magazynowana i przetwarzana na np. kwas siarkowy (H2SO4) do celów przemysłu chemicznego, węgiel mógłby zostać użyty w celu produkcji tworzyw sztucznych, bądź w celu produkcji benzyny syntetycznej.
Z drugiej strony obecna brudna chemia nie szybko ustąpi miejsca swoim lepszym stronom, bo siłą rzeczy technologia opiera się na węglu i dopóki on będzie - będzie wykorzystywany, gdyż jest on stosunkowo łatwy do pozyskania a to determinuje późniejsze rozwiązania na których stoi obecny przemysł i każdy kto próbuje to zmienić w radykalny sposób eliminując tą sytuację będzie postrzegany jako radykalny głos i nie zostanie udzielony mu poważniejszy udział w sferze decyzyjnej. Za kilkaset, a może nawet już tylko za kilkadziesiąt lat będzie musiał nastąpić nieuchronny odwrót na całej linii frontu z paliw jakie znamy, bo ceny ich na skutek gwałtownego zmniejszania się ich zasobów w niedalekiej przyszłości wzrosną tak, że nikt nie będzie w stanie utrzymać samochodów, które staną się tylko zabawkami dla ekscentrycznych bogaczy, których będzie na nie stać. Nie będzie też miejsca na elektrownie opalane węglem ani innymi paliwami kopalnymi, a prąd będzie wytwarzany ze źródeł, które obecnie tylko dopiero zarysowują się na horyzoncie technologicznym współczesności. Jakie to będą źródła zależne będzie od wielu wydarzeń, które nastąpią, a których nie sposób obecnie przewidzieć.
Inne technologie nie oparte na spalaniu węglopochodnych paliw są w mniejszości w porównaniu z globalną produkcją energii. Cykle przyrodnicze typu cyklu z udziałem światła, czyli fotosyntezy będące w równowadze z produkowanym na różne sposoby dwutlenkiem węgla w przeszłości spowodowały wydzielenie go z atmosfery i obecnie w postaci węgla kamiennego i brunatnego zalega on pod Ziemią.Poprzez wydobycie go w procesie prac górniczych i spalanie dochodzi do powrotu tego gazu do atmosfery, co może być w dłuższej perspektywie czasowej przyczyną tego, że następne pokolenia będą zmuszone do wypracowania innych technik pozyskania energii, jeżeli będą chciały przetrwać. Skażenie wód powierzchniowych jest także znaczne, szczególnie śródlądowych. Woda morska jest zanieczyszczona przy wybrzeżach, gdzie ujście mają delty rzek. Tlenki siarki (SO2, SO3) oraz azotu (NO2) zakwaszają hydrosferę. Są miejsca na planecie gdzie zatrucie środowiska przekracza wszelkie normy, pomimo tego żyją tam ludzie, gdyż organizm ludzki może przystosować się jeżeli będzie przyzwyczajany do trujących substancji stopniowo. W atmosferze jest coraz więcej wilgoci i oparów. Na moim osiedlu jesienią i w zimie praktycznie nie można otworzyć okna, zwłaszcza przy bezwietrznej pogodzie, bo powietrze jest tak zanieczyszczone z palenisk opalanych węglem i innymi substancjami, że trudno oddychać. Sytuacja mogłaby ulec zmianie, gdyby można było domknąć cykl produkcji spalin poprzez nie magazynowanie ich pod ziemią, a poprzez przerobienie ich za pomocą sztucznej fotosyntezy z powrotem na tlen i węgiel albo metan, które mogły by po raz kolejny być spalone i cykl by się domknął.
Do tego celu można by również zastosować np. reakcję Sabatiera katalizowaną przez ruten lub reakcje typu Fischera-Tropscha w celu otrzymania węglowodorów z CO i H2. Inne metody to kolejne technologie określane jako tkz. "Green chemistry" polegającą na bezodpadowych reakcjach chemicznych, w procesie których nie powstają produkty uboczne. Większość procesów chemicznych zachodzących w przyrodzie może być wzorcem dla wielu rozwiązań technologicznych w chemii przemysłowej. Adaptacja niektórych z nich to poważne wyzwanie dla nauki. Obieg podstawowych elementów w przyrodzie napędza energia słoneczna. Energia słoneczna, której faktycznie jeżeli brać pod uwagę całkowitą jej wartość produkowaną przez Słońce, a która dociera do Ziemi, jest znikomo mała, reszta marnuje się i jest rozpraszana w bezkresie przestrzeni Układu Słonecznego. Są to wartości energii, którą gdyby udało się jakoś wykorzystać np. magazynując ją w jakichś kryształach, mogła by umożliwić napędy typu WARP i inne obecnie nie stosowane idee z uwagi na ich wymogi technologiczne. Energia produkowana przez elektrownie na świecie, jest wytwarzana z małą sprawnością, na każdym elemencie typu turbiny, prądnicy, generatora pary, następują opory bezwładnościowe i dynamiczne powodujące duże straty energii. .
W przyrodzie fotosynteza zachodzi z udziałem cząsteczki chlorofilu z centralnie położonym atomem magnezu z udziałem światła widzialnego, przy niskich energiach aktywacji progu energetycznego reakcji. Sztuczna fotosynteza w postaci, którą postuluje się obecnie jest procesem o wiele bardziej wymagającym energetycznie, podczas gdy reakcja w przyrodzie zachodzi łatwo, tutaj musimy dostarczyć energii ultrafioletu, czyli energii fali wyższej niż światło widzialne. Skutecznego katalitycznego użycia innych niż chlorofil substancji jak rodopsyna jest wiele i chemia jest bogata w ciekawe rozwiązania zastępcze fotosyntezy, jednak nie widać na razie praktycznego użycia tych technologii na skalę przemysłową, ze szczególnym naciskiem w kierunku "odtrucia" atmosfery z nadmiaru CO2. Innym ciekawym zastosowaniem m.in. biotechnologii, byłoby zastosowanie procesów przyrodniczych do napędu pojazdów w cyklu zamkniętym, z udziałem odpowiednich reakcji chemicznych, które zapewniałyby odzysk spalonego paliwa ze spalin, czyli w tym rozwiązaniu zero emisyjnym, zakładając 100 % sprawności reakcji, byłoby to rozwiązanie typu "free energy". Jednak gdyby rozważać tego typu rozwiązania gdzie tankowanie paliwa, byłoby jednorazową czynnością i później można by jeździć do całkowitego zużycia mechanicznego elementów samochodu, to całość zakrawa już na fantastykę i może być obiektem zainteresowania pisarzy sci-fi. Kiedyś spotkałem się także z opisem urządzeń, które teoretycznie funkcjonują na zasadzie obdzierania z elektronów cząstek powietrza, energia uzyskana tym sposobem miałaby być użyta do zasilania nawet mocno prądożernych urządzeń. Urządzenie tego typu powodowało powstawanie O3 w swoim otoczeniu jako jedyny skutek uboczny jego pracy. Jeżeli chodzi jednak o CO2 to najwięcej zanieczyszczeń emitują koksownie oraz huty - gdzie w procesie przeróbki rudy na stal przy jej redukcji musi utleniany być węgiel, a produktem odpadowym jest dwutlenek węgla. Innymi producentami CO2 są cementownie, bo w procesie uzyskania cementu czy wapna, w produkcji którego powstaje dwutlenek węgla z margla, który składa się w dużej części CaCO3, czyli węglanu wapnia, nie można wyeliminować procesów z produktami końcowymi, z którymi nie wiadomo co zrobić. Innym problemem jest powstawanie dużych ilości popiołów z elektrowni z kotłami węglowymi, ale również na biomasę i spalarni spalających śmieci. .
Wszystkie gazy toksyczne emitowane z palenisk piecowych można rozbić na molekuły podstawowe tj. tlenki azotu, na tlen i azot, przy użyciu katalizatorów, tlenki siarki i węgla po części nie są składnikiem powietrza jak w przypadku tlenków azotu, więc siarka musiałaby być magazynowana i przetwarzana na np. kwas siarkowy (H2SO4) do celów przemysłu chemicznego, węgiel mógłby zostać użyty w celu produkcji tworzyw sztucznych, bądź w celu produkcji benzyny syntetycznej.
Z drugiej strony obecna brudna chemia nie szybko ustąpi miejsca swoim lepszym stronom, bo siłą rzeczy technologia opiera się na węglu i dopóki on będzie - będzie wykorzystywany, gdyż jest on stosunkowo łatwy do pozyskania a to determinuje późniejsze rozwiązania na których stoi obecny przemysł i każdy kto próbuje to zmienić w radykalny sposób eliminując tą sytuację będzie postrzegany jako radykalny głos i nie zostanie udzielony mu poważniejszy udział w sferze decyzyjnej. Za kilkaset, a może nawet już tylko za kilkadziesiąt lat będzie musiał nastąpić nieuchronny odwrót na całej linii frontu z paliw jakie znamy, bo ceny ich na skutek gwałtownego zmniejszania się ich zasobów w niedalekiej przyszłości wzrosną tak, że nikt nie będzie w stanie utrzymać samochodów, które staną się tylko zabawkami dla ekscentrycznych bogaczy, których będzie na nie stać. Nie będzie też miejsca na elektrownie opalane węglem ani innymi paliwami kopalnymi, a prąd będzie wytwarzany ze źródeł, które obecnie tylko dopiero zarysowują się na horyzoncie technologicznym współczesności. Jakie to będą źródła zależne będzie od wielu wydarzeń, które nastąpią, a których nie sposób obecnie przewidzieć.





